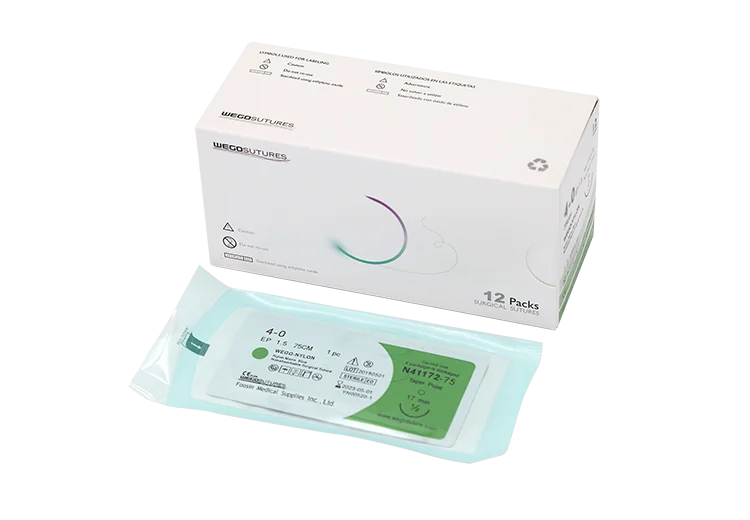
考虑外科缝合线的复杂旅程,从原材料到在人体内部闭合伤口的无菌设备。这个过程不是由偏好决定的,而是由一套严格的强制性规则框架所定义。对于任何外科缝合线制造商来说,遵守这些合规标准是运营和市场准入的绝对基础。在WEGO医疗,我们的流程围绕这一框架构建,确保每个产品都能履行其关键职责。.
遵守国际质量管理体系
合规制造的基础是经过认证的质量管理体系(QMS)。像ISO 13485这样的标准规定了专门针对医疗设备的全面系统的要求。对于一个 外科缝合线制造商, ,这转化为对每一个阶段的文档化程序的管理:从初始设计控制和供应商资格到细致的过程验证和最终产品发布。该系统确保了一致性和可追溯性。这意味着每批材料都有记录,每个灭菌周期都经过验证,每个不合格项都要进行调查。WEGO医疗维护的强大QMS提供了可预测、高质量输出所需的结构化环境。.
满足地区监管指令和许可
虽然QMS提供了运营的支柱,但市场授权要求特定的监管合规性。不同地区执行各自的指令。在欧盟,缝合线必须在医疗器械法规(MDR)下带有CE标志,以证明符合健康、安全和性能要求。在美国,外科缝合线制造商必须获得食品和药物管理局的许可,通常通过510(k)提交证明与前体设备的实质等同性。这些不是一次性的成就,而是对市场后续监测、报告和质量审计的持续承诺。导航这一领域是像WEGO医疗这样的负责任制造商的核心职能。.
验证材料安全性和灭菌保证
合规性直接与材料科学和微生物学交叉。存在标准以证明两个不可谈判的要点:生物安全性和无菌性。生物相容性测试——评估缝合材料与活组织的相互作用——遵循严格的ISO 10993协议。此外,证明所选灭菌方法(如环氧乙烷或伽马辐射)始终达到10^-6的灭菌保证水平(SAL)是强制性的。这需要在最坏情况下挑战过程的详尽验证研究。对于外科缝合线制造商来说,这种科学验证是产品安全用于其预期用途的证据。.
合规的领域复杂且不可谈判。它将管理理念、监管法律和严格的科学验证整合为统一的控制策略。这些标准的存在是为了将简单的线变成可靠、可预测的医疗设备。对于医疗服务提供者来说,这一基础设施提供了信心。在 威高医疗, ,将这些标准视为质量的基本蓝图而非障碍,是我们日常纪律和对该领域长期承诺的指导。.